7月份中美歐批準上市新(xīn)藥盤點
發布日期:2022-08-24 閱讀次數:11493 來源:中國(guó)食品藥品網
摘要:
7月份,中美歐共批準6款新(xīn)藥上市。其中,中國(guó)和歐盟各有3款新(xīn)藥獲批,美國(guó)無新(xīn)藥獲批。
我國(guó)批準3款新(xīn)藥上市
7月份,我國(guó)共批準3款新(xīn)藥上市(詳見表1),其中附條件批準的普特利單抗為(wèi)我國(guó)藥企樂普生物(wù)自主研發。

普特利單抗是通過使用(yòng)人IgG4亞型針對人PD-1的人源化單抗。它可(kě)以拮抗PD-1信号,通過阻斷PD-1與其配體(tǐ)PD-L1、PD-L2的結合來恢複免疫細胞殺死癌細胞的能(néng)力,用(yòng)于既往接受一線(xiàn)及以上系統治療失敗的微衛星高度不穩定(MSI-H)/錯配修複功能(néng)缺陷(dMMR)實體(tǐ)瘤患者的治療。同時,普特利單抗采用(yòng)抗體(tǐ)工程技(jì )術,于Fc區(qū)引入突變,提高FcRn受體(tǐ)的結合親和力,從而大幅延長(cháng)其半衰期,提高患者的臨床療效及藥物(wù)依從性。在2021年美國(guó)臨床腫瘤學(xué)會(ASCO)會議上,樂普生物(wù)公布了普特利單抗用(yòng)于MSI-H/dMMR實體(tǐ)瘤的多(duō)中心Ⅱ期臨床試驗結果。結果顯示,在納入的100名二線(xiàn)及以上患者中,86例達到初步反應評價。研究主要終點客觀緩解率(ORR)達到47.67%,疾病控制率(DCR)為(wèi)75.58%,6個月和12個月無進展生存期(PFS)率分(fēn)别為(wèi)62.66%和52.70%。
恩曲替尼是羅氏研發的針對NTRK和ROS1基因融合而設計的特異性酪氨酸激酶抑制劑。NTRK融合陽性腫瘤産生的原因是NTRK1/2/3基因與其他(tā)基因融合,導緻編碼的TRK蛋白(TRKA/B/C)出現異常,激活與特定癌症增殖相關的信号通路。NTRK基因融合可(kě)能(néng)出現在起源于身體(tǐ)不同位置的腫瘤中,包括乳腺癌、膽管癌、非小(xiǎo)細胞肺癌等。恩曲替尼治療NTRK融合陽性局部晚期或轉移性實體(tǐ)瘤的效果,已在多(duō)項臨床試驗中證明對多(duō)達10種不同類型的實體(tǐ)瘤患者有響應。
曲拉西利是先聲藥業引進的由美國(guó)公司G1 Therapeutics開發的一款短效細胞周期蛋白依賴性激酶4和6(CDK4/6)抑制劑。CDK4/6被認為(wèi)是驅動細胞分(fēn)裂的關鍵調節因子,它通過與一類叫細胞周期蛋白(cyclinD)的蛋白質(zhì)結合,磷酸化視網膜母細胞瘤蛋白(Rb),釋放轉錄因子E2F,進而促進細胞周期相關基因的轉錄,使細胞周期從DNA合成前期(G1期)進入到DNA複制期(S1期)。曲拉西利通過短暫的G1期阻滞,降低骨髓造血幹細胞的複制負擔,從而緩解骨髓造血幹細胞的耗竭。曲拉西利曾獲美國(guó)食品藥品管理(lǐ)局(FDA)授予突破性療法認定和優先審評資格,并于2021年2月獲FDA批準上市。2020年8月,先聲藥業與G1 Therapeutics達成授權合作(zuò),獲得了在大中華區(qū)對曲拉西利所有适應症的開發和商業化權益。
歐盟批準3款新(xīn)藥上市
根據Pharmadigger數據庫數據,7月份,歐盟共批準3款新(xīn)藥上市(詳見表2)。其中,Eladocagene exuparvovec為(wèi)全球首次獲批。
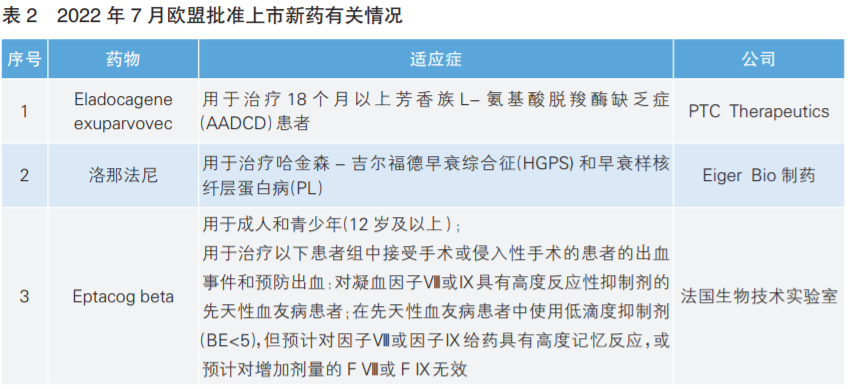
Eladocagene exuparvovec是美國(guó)公司PTC Therapeutics開發的基于腺相關病毒2(AAV2)載體(tǐ)并能(néng)直接注入大腦的首款獲批基因療法,用(yòng)于治療18個月以上芳香族L-氨基酸脫羧酶缺乏症(AADCD)患者。AADCD是一種緻命的罕見遺傳病,患者由于編碼AADC酶的多(duō)巴脫羧酶(DDC)基因出現變異,導緻AADC酶功能(néng)缺失。通常患者出生幾個月内就會出現嚴重運動障礙,包括運動功能(néng)減退、肌張力障礙等,嚴重影響生活。這一基因療法通過一次性治療,将功能(néng)正常的DDC基因直接遞送到患者大腦的殼核中,從而提高AADC酶的水平并恢複多(duō)巴胺的生産。
洛那法尼是美國(guó)制藥公司Eiger Bio研發的一種口服法尼基轉移酶抑制劑,其通過抑制早衰蛋白的異戊二烯化,進而降低早衰蛋白在細胞核中的積累,用(yòng)于一種極罕見且具有緻命性的遺傳病——早衰症的治療。該藥最早于2020年11月獲得美國(guó)FDA批準上市。
Eptacogbeta是法國(guó)生物(wù)技(jì )術實驗室研發的重組人凝血因子Ⅶa類似物(wù)。該藥物(wù)最早于2020年4月獲得美國(guó)FDA批準上市。














